

栏目分类
发布日期:2024-11-18 16:11 点击次数:114
大家平时经常说的“血脂高、胆固醇高”,在医学上都属于血脂异常。
据统计,中国成人血脂异常(包括高胆固醇血症、高甘油三酯血症、混合型高脂血症和低高密度脂蛋白胆固醇血症)的总体患病率高达35.6%,其中低密度脂蛋白胆固醇(LDL-C)俗称“坏胆固醇”,是心血管事件独立的致病性危险因素,也是降胆固醇治疗的首要目标。血脂异常初期往往没有明显不适,但随着疾病进展,会显著增加动脉粥样硬化性心血管疾病(ASCVD)风险,也是导致中国居民死亡的首要原因。
随着血脂异常患者逐年增多,他汀类药物等传统降脂药已经被越来越多人熟知。他汀类药物是降LDL-C治疗的首选,中等强度的他汀类药物可以降低LDL-C水平约30%~50%。
但他汀类药物并不是“万能的”。对于大部分动脉粥样硬化性心血管疾病患者而言,尽管用了中等强度的他汀类药物,但血脂仍然难以达到目标值。研究显示,他汀类药物剂量即使在初始剂量基础上翻倍,进一步的降脂幅度也仅为6%。这也被科学界称为“他汀的瓶颈”。
另外,由于他汀类药物每天都要服用,时间长了容易漏服或不按时服药,治疗效果也会打折扣(影响长期依从性),还有一些患者对他汀类药物存在不耐受的问题。
为了解决这些问题,科学家开发出了更长效、更安全的治疗药物,比如新型降胆固醇药物——前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂。在不同的患者群体中(不管是家族性还是非家族性高胆固醇血症),无论之前是否使用过他汀类药物治疗,这类疗法均能将LDL-C水平持续降低50%~70%,并能改善心血管结局。
近几年,PCSK9抑制剂在脂质异常疾病方面已取得较大进展。现有的PCSK9抑制剂通常是每两周或每月一次注射给药,而其中有一款今年在中国获批的新药英克司兰钠注射液,甚至可以做到“打一针管半年”。
今天,带大家来认识下这款“超长效”降脂药。
打一针就能管半年,这款新型降脂药可将“坏胆固醇”水平降低60%
研究表明,PCSK9基因的活跃表达会促进低密度脂蛋白受体(LDLR)的降解,从而降低肝脏清除血液中胆固醇的能力,这可能导致“坏胆固醇”水平长期升高。而PCSK9抑制剂能直接阻止循环中PCSK9与LDLR相结合,减少PCSK9介导的LDLR的分解,加强其对“坏胆固醇”的清除能力。
我们开头提到“打一针管半年”的英克司兰钠注射液(inclisiran,商品名:乐可为),就是一款靶向PCSK9的小干扰RNA(siRNA)疗法,作为siRNA疗法,它的特点是可直接与编码PCSK9蛋白的mRNA结合,通过RNA干扰作用降低mRNA的水平,从而防止肝脏生成PCSK9蛋白。PCSK9蛋白的作用是抑制LDLR的回收和再利用。因此,降低PCSK9蛋白的水平可以让更多LDLR回到肝细胞表面,与更多LDL结合,将它们从血液中清除。当英克司兰进入肝细胞后,会形成囊泡长期存在,也就是形成独特的“胞内缓释系统”,缓慢释放可达数月,长期降脂。
重要的是,患者只需在初次给药后3个月时给药一次,之后只需要每半年给药一次,用药的便捷性大幅提高。从用药频次来看,每年注射两次即可降低LDL-C水平,是一款长效降脂药物,有助于提升治疗依从性,进行血脂的长期管理。
这款新药已分别于2021年12月和2023年8月在美国和中国获批上市,适应症为作为饮食的辅助疗法,用于成人原发性高胆固醇血症(杂合子型家族性和非家族性)或混合性血脂异常患者的治疗,包含:
在接受最大耐受剂量的他汀类药物治疗仍无法达到LDL-C目标的患者中,与他汀类药物,或者与他汀类药物及其他降脂疗法联合用药;
以及在他汀类药物不耐受或禁忌使用的患者中,单独用药或与其他降脂疗法联合用药。
今年4月,在第73届美国心脏病学会科学年会(ACC 2024)上,这款新药的一项关键研究结果被公布出来,结果显示,在接受最大耐受他汀类药物治疗且血脂控制不佳的ASCVD患者中,相比常规治疗,“加用英克司兰”(“inclisiran-first”)策略(在接受最大耐受他汀类药物治疗且未能达到LDL-C<70 mg/dL的情况下,立即加用英克司兰治疗)可以更大幅度降低LDL-C,在随访330天时降幅高达60.0%。
这项3b期试验纳入了年龄≥18岁、既往单独接受最大耐受他汀类药物治疗、LDL-C≥70 mg/dL或非高密度脂蛋白胆固醇(non-HDL-C)≥100 mg/dL的ASCVD患者,并将450例患者按1:1比例随机分配至“加用英克司兰”组(英克司兰+常规治疗,225例)或常规治疗组(根据研究者判断进行的其他降脂治疗,225例)。患者中位年龄为67岁,其中30.9%为女性。
在随访330天期间发现:
与常规治疗(降低7.0%)相比,“加用英克司兰”策略使LDL-C在第330天时相较于基线显著降低60.0%。此外,“英克司兰”组的他汀类药物停药率并不劣效于常规治疗组(6.0% vs. 16.7%)。
在次要结局方面,第330天时,“英克司兰”组与常规治疗组相比,有更多患者达到了LDL-C目标,且两组安全性相似:
两组患者中,LDL-C降幅≥50%的患者比例分别为69.8%和5.3%。而达到LDL-C<70 mg/dL及LDL-C<55 mg/dL降脂目标的患者比例分别为81.8% vs. 22.2%及71.6% vs. 8.9%。
此外,两组患者复合主要心血管不良事件(MACE)的发生率相似,分别为:2.7%和2.2%。
总体来说,在接受最大耐受他汀类药物治疗且血脂控制不佳的ASCVD患者中,与常规治疗相比,“加用英克司兰”策略使LDL-C更低,同时也没有阻碍他汀类药物的使用或引起新的安全问题。
需要提醒的是,这项研究中的治疗组患者并没有停用他汀类药物,而是在此基础上加用了英克司兰。所以研究中的患者仍然需要每天吃他汀类药物,还没有真正做到“只需每半年打一针、不用每天吃药”。
目前这款药物获批的适应症也是以联合用药为主,只对部分特殊患者考虑单独用药。但相信随着医药研究的进步,或许今后真的能实现“所有血脂异常患者都不用天天吃药”。
降脂药物的发展史
从20世纪初科学家们开始胆固醇的相关研究,到20世纪70年代以来多种降脂疗法的陆续诞生,降脂药物的发展经过了一百多年的历史。
1901年,德国著名化学家阿道夫•温道斯(Adolf Windaus)开始进行胆固醇和相关类固醇结构的研究和测定工作。1904年,德国病理学家费利克斯•马尔尚(Felix Marchand)首次提出“动脉粥样硬化”的概念。后来科学家逐步明确,血液中的高胆固醇水平与冠心病有关。直到20世纪50年代,美国科学家明确了“坏胆固醇”是引起冠心病的主要原因。同一时期,胆固醇的生物合成研究也取得重大进展。
这些关于胆固醇的发现,不仅诞生了3个诺贝尔奖,还为后来降脂药物的研发奠定了基础。

1. 他汀类药物开发的时代
1973年,后来被誉为“他汀药物之父”的日本科学家远藤章(Akira Endo),从一种叫“桔青霉”的菌类中成功提取了能抑制胆固醇合成的活性化合物,代号为ML-236B(也就是后来的美伐他汀),这也是史上首个羟甲基戊二酰辅酶A(HMG-CoA)还原酶抑制剂。但由于种种原因,这个化合物最终没能被继续开发上市。
1979年,远藤章又从某种红曲霉菌中分离出了一种HMG-CoA还原酶抑制剂,在分子结构上仅比美伐他汀多了一个甲基;同一时期,默沙东也从另一种真菌中发现了同样的化合物。这就是后来的洛伐他汀,于1987年在美国获批上市。洛伐他汀(Mevacor,商品名:美伐克)也是第一个上市的他汀类药物。
从20世纪90年代到21世纪初期,又有一系列他汀类药物相继问世,包括辛伐他汀、普伐他汀、氟伐他汀等。
其中,第一代产品洛伐他汀直接来源于天然产物;而第二代产品辛伐他汀、普伐他汀是第一代的衍生物;第三代产品氟伐他汀、阿托伐他汀、瑞舒伐他汀、匹伐他汀则属于人工合成的他汀类药物。
与第一代和第二代他汀相比,第三代他汀的优势是降脂效果更好,半衰期更长(也就是一次服药后药效持续时间更长,可以减少服药次数),且肝肾毒性更低。
他汀类药物的问世,在人类ASCVD防治史上具有里程碑式的意义。据统计,他汀类药物能够显著降低“坏胆固醇”含量(25%-35%),以及降低心血管疾病发病率(25%-30%)和死亡率(~30%)。
2. 后他汀时代
前面已经提到,他汀类药物也存在一些瓶颈和耐受性的问题。为了克服这些难题,胆固醇吸收抑制剂、PCSK9抑制剂、ATP柠檬酸裂解酶(ACL)抑制剂、siRNA疗法等新一代降脂疗法又相继出现在药物开发的舞台。
(1) 胆固醇吸收抑制剂
21世纪初期,以依折麦布为代表的选择性胆固醇吸收抑制剂问世,为降胆固醇药物的联合应用提供了新方案。
这类药物可作用于肠道和肝细胞表面的尼曼-匹克C1型类似蛋白1(Niemann-PickC1-like1,NPC1L1)受体,选择性地抑制胆固醇的吸收,从而降低小肠中胆固醇向肝脏转运,降低肝脏胆固醇贮量,降低血液中胆固醇量。此外,这种作用机制可与他汀类的作用互补,通过联合用药能更有效改善多种胆固醇水平。
依折麦布(商品名:益适纯)分别于2002年、2006年在美国和中国获批上市。研究证实,依折麦布与他汀类药物联用,也就是在他汀类药物治疗基础上加用依折麦布,可使LDL-C水平进一步降低18%~25.8%,从而显著提高血脂达标率,但其不良反应发生率与单独应用他汀类药物时无显著差别。
2021年,中国国产的1类创新药海博麦布(商品名:赛斯美)也在中国获批上市,其作用机制和依折麦布相似,它的上市为原发性高胆固醇血症患者提供了新的治疗选择。
(2)PCSK9抑制剂
PCSK9抑制剂被认为是继他汀后的新一代降脂药物。
2003年,阿比法德尔(Abifadel)等在家族性高胆固醇血症的患者中发现了编码PCSK9的基因突变;后来又有研究表明,PCSK9功能缺失突变与较低的LDL-C水平及冠心病发病率相关,而功能获得突变会导致蛋白质功能过表达,并与家族性高胆固醇血症及心血管事件风险增加相关。经过20年的发展,如今PCSK9已成为创新药研发领域的一个备受瞩目的靶点。
2015年7月,美国食品药品监督管理局(FDA)批准阿利西尤单抗(商品名:波立达)注射液,这是在美国获批的首个PCSK9抑制剂类降脂药物,并于2020年在中国获批上市;2015年8月,第二款PCSK9抑制剂依洛尤单抗(商品名:瑞百安)也获得美国FDA批准,并于2018年在中国获批。
2020年,本文开头提到的siRNA疗法英克司兰在欧洲获得全球首批,用于治疗成人高胆固醇血症及混合性血脂异常。
除了英克司兰,目前其他5款PCSK9抑制剂也已在中国获批上市,还有多款药物已进入关键临床试验阶段。
与此同时,多款靶向PCSK9的创新降脂疗法正在临床开发中,比如RNAi疗法ARO-APOC3,旨在通过降低靶向载脂蛋白C3(APOC3)蛋白的表达水平,在降低甘油三酯水平和极低密度脂蛋白水平的同时,提升高密度脂蛋白水平。
在上述药物之外,科学家还发现了促进LDL清除的普罗布考、阻断肠道内胆汁酸中胆固醇的重吸收的胆酸螯合剂;主要用于降低甘油三酯水平的贝特类药物、高纯度ω⁃3脂肪酸和烟酸类药物;以及作用于新靶点的降脂药物,如三磷酸腺苷(ATP)柠檬酸裂解酶抑制剂贝派地酸(bempedoicacid)、血管生成素样蛋白3全人源单抗evinacumab、ApoC3抑制剂volanesorsen、以及降低脂蛋白(a)的新药,包括载脂蛋白(a)反义寡核苷酸(pelacarsen)和载脂蛋白(a)小干扰RNA(SLN360)等。
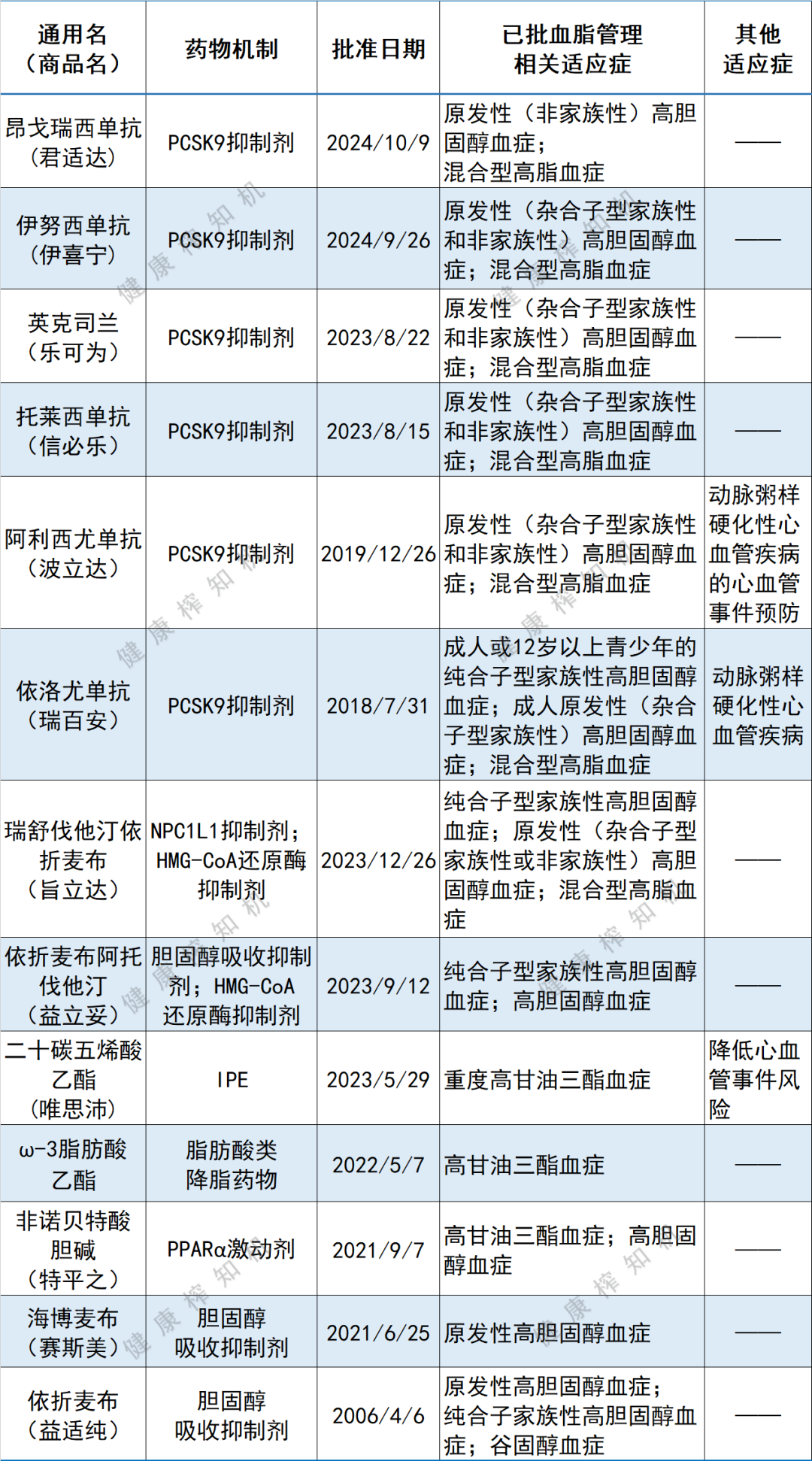
自2006年4月以来,获中国国家药品监督管理局(NMPA)批准用于血脂管理的药物如下:
上一篇:没有了
下一篇:没有了